细胞异质性是所有生物体中普遍存在的现象。关于细胞异质性的信息主要通过单细胞分析获得,这有助于进一步了解生命活动的性质和内部机制。细胞中的蛋白质组学差异是细胞异质性的重要表现,并为进一步的研究提供了方向。蛋白质是细胞生长、分裂、信号转导和催化生化过程的重要组成部分。此外,细胞蛋白的表达水平与mRNA含量、癌症的发生发展和特异性细胞活性密切相关。细胞中不同蛋白的表达水平之间存在着一定的内在关系。然而,其相互作用的机制尚不完全清楚,这需要同时对多种蛋白质进行定量分析。因此,对单个细胞内多中蛋白质的同时定量分析对于了解细胞蛋白质组学的作用机制具有重要意义。
DNA步行器是一种具有广泛应用潜力的技术,已广泛应用于生物传感和成像分析。用DNA步行器构建的纳米探针可以大大提高检测方法的灵敏度,具有良好的特异性,特别是基于金纳米颗粒的DNA步行器,可以实现核酸信号的扩增,从而大大提高核酸检测方法的灵敏度。此外,利用DNA碱基互补性的原理,蛋白质的适配体可以在金纳米颗粒上进行修饰,可以实现多组份同时信号扩增,并对蛋白质的检测保持良好的特异性。
微流控芯片电泳技术因其操作简单、灵敏度高、集成度高等优点而备受广泛关注,并被广泛应用于单细胞中生物活性分子的定量分析。然而,能够同时定量单个细胞中多种微量蛋白的微流控技术目前还少有报道。主要原因包括肿瘤相关蛋白含量低,来自其它细胞成分的干扰严重,以及缺乏能够直接定量单个细胞中多种蛋白的方法。因此,要实现单个细胞中多种肿瘤相关微量蛋白的同时定量,发展基于微流控芯片电泳平台的多组份同时信号放大策略、建立灵敏度高,特异性好的单细胞中多种微量蛋白同时定量的方法,是其关键技术之一。
最近,广西师范大学的赵书林教授(点击查看介绍)团队提出了一种细胞内多组分同步DNA行走策略,基于微流控芯片平台,实现了单个细胞中两种肿瘤相关蛋白的同时定量。在他们的研究中,设计了一种多元DNA步行荧光纳米探针,用于同时定量两种癌症相关蛋白:核仁蛋白(NCL)和胸腺苷激酶1(TK1)。NCL和TK1的测定有助于监测实体肿瘤和血液系统恶性肿瘤的发生和发展情况。使用设计的纳米探针对NCL和TK1进行细胞内同时信号放大,并在微芯片电泳平台上,采用激光诱导荧光(MCE-LIF)法分别检测20个HepG2细胞和20个HL-7702细胞中NCL和TK1的含量。该方法具有高灵敏度和特异性,可用于单细胞中NCL和TK1的同时绝对定量分析。此外,利用合理的DNA序列设计,可以在单个细胞中完成对其它蛋白质或多个蛋白质的绝对定量。它有望成为单细胞分析的良好技术平台,其方法原理如下图所示。
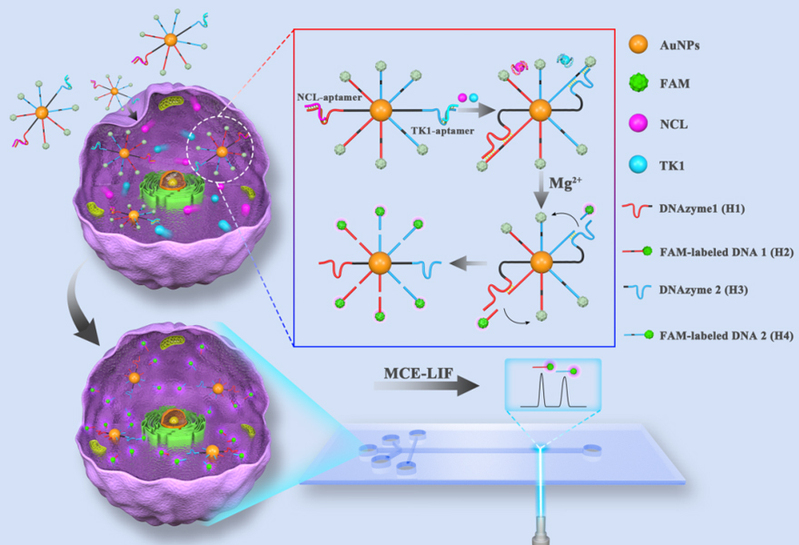
图1. 细胞内多组分同步DNA行走策略定量检测NCL和TK1
作者使用该策略,分析了20个HL-7702细胞和20个HepG2细胞。下图A和B是三个HL-7702细胞和三个HepG2细胞的典型电泳图。电泳曲线显示:同一个细胞中NCL和TK1能完全分离,在同一类型细胞中NCL和TK1的峰面积不同。在不同类型细胞中NCL和TK1的峰面积相差较大,说明了细胞中蛋白质组的异质性。20 个HepG2细胞和20 个HL-7702细胞中NCL和TK1含量的绝对定量结果如下图C、D、E和F所示。HepG2细胞中NCL和TK1的平均含量分别为43.7±3.5 zmol/cell 和55.1±5.6 zmol/cell,而HL-7702细胞中NCL和TK1的平均含量分别为4.98±0.68 zmol/cell 和9.44±1.36 zmol/cell。HepG2细胞中NCL和TK1的平均水平约为HL-7702的8.7倍和5.8倍,表明HepG2细胞中NCL和TK1的水平显著高于HL-7702。这些测定结果证明NCL和TK1是重要的肿瘤标志物,在肝癌中过表达。在同一类型细胞中,细胞之间NCL和TK1的含量也有较大差异。因此,通过对单个细胞中的NCL和TK1的分析,可以进一步了解细胞中蛋白组的差异,这对研究蛋白质与肝癌之间的关系具有重要意义。此外,在单个细胞中同时定量多个蛋白,对于深入了解细胞蛋白的生物学作用提供了见解。
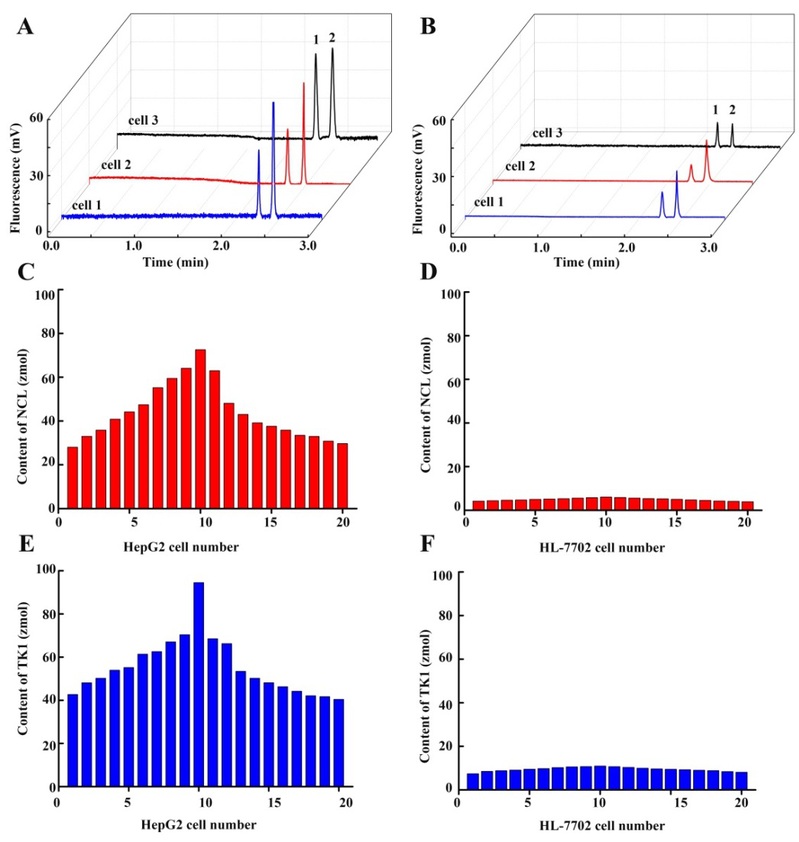
图2. (A) 3个HepG2细胞的典型电泳图。峰识别:1. NCL, 2.TK1. (B) 3个HL-7702细胞的典型电泳图。峰识别:1. NCL, 2. TK1. (C) 20个HepG2细胞中NCL的含量 (zmol/cell)。 (D) 20个HL-7702细胞中NCL的含量 (zmol/cell)。(E) 20个HepG2细胞中TK1的含量 (zmol/cell)。(F) 20个HL-7702细胞中TK1的含量 (zmol/cell)。
这一成果近期将以封面文章发表在Analytical Chemistry 上,文章的第一作者是广西师范大学的博士研究生陈盛余,相关研究工作得到国家自然科学基金项目的资助。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Intracellular Multicomponent Synchronous DNA-Walking Strategy for the Simultaneous Quantification of Tumor-Associated Proteins in a Single Cell
Shengyu Chen, Jingjin Zhao*, Chunhuan Xu, Liangliang Zhang, Bingfang Shi, Jianniao Tian, and Shulin Zhao*
Anal. Chem., 2022, DOI: 10.1021/acs.analchem.2c03771
导师介绍
赵书林
https://www.x-mol.com/university/faculty/9780


